Kit de teste rápido de antígeno para adenovírus aprovado pela CE
1. USO PREVISTO
Este kit é aplicável à detecção qualitativa in vitro de antígeno de adenovírus (AV) que pode existir em amostras de fezes humanas, o que é adequado para auxiliar no diagnóstico de infecção por adenovírus em pacientes com diarreia infantil.Este kit fornece apenas resultados de teste de antígeno de adenovírus e os resultados obtidos devem ser usados em combinação com outras informações clínicas para análise.Deve ser utilizado apenas por profissionais de saúde.
2. ESPECIFICAÇÃO DO PRODUTO
| Nº do modelo | AV |
| Metodologia | ouro coloidal |
| Tipo de amostra | Rostos |
| Hora do resultado | 10-15 minutos |
| Armazenar | 2~30 ℃/36~86 ℉ |
| Validade | 24 meses |
| Certificado | ISO13485, Certificado CE, Certificado UCKA MHRA |

| COMPONENTES PRINCIPAIS DO KIT * Dispositivo de teste * Tubo de coleta de amostras * Pipeta descartável * Instruções de uso | EMBALAGEM * 20 teste/kit * Rotulagem de saco de folha de alumínio * embalar a vácuo
|
3. MÉTODO DE TESTE
| 1 | Use o tubo de amostragem para coleta de amostra, mistura completa e diluição para uso posterior.Use bastão de prova para tirar aprox.30 mg de fezes, coloque-o no tubo de amostragem carregado com diluente de amostra, aperte bem a tampa e agite-o bem para uso posterior. |
| 2 | No caso de fezes finas de pacientes com diarreia, use uma pipeta descartável para pipetar a amostra e adicione 3 gotas (aprox. 100μL) da amostra gota a gota ao tubo de amostragem e agite bem a amostra e o diluente da amostra para uso posterior. |
| 3 | Remova o dispositivo de teste da bolsa de papel alumínio, coloque-o em uma bancada horizontal e faça um bom trabalho na marcação. |
| 4 | Descarte as duas primeiras gotas da amostra diluída, adicione 3 gotas (aprox. 100μL) da amostra diluída sem bolhas gota a gota no poço do dispositivo de teste vertical e lentamente e comece a contar o tempo. |
| 5 | Interprete o resultado dentro de 10 a 15 minutos e o resultado da detecção é inválido após 15 minutos (consulte os resultados detalhados na interpretação do resultado). |
4. AVALIAÇÃO E EXPLICAÇÃO DO RESULTADO
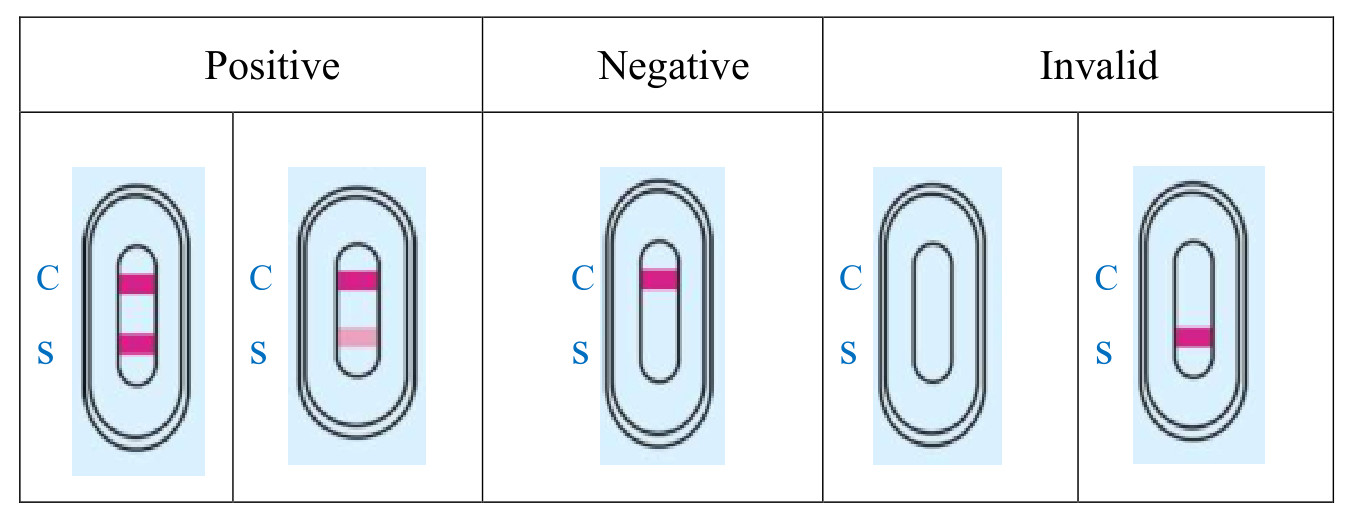
5. DESEMPENHO CLÍNICO
O desempenho clínico deste produto é avaliado por meio da coleta de 276 casos de amostras clínicas.Kit comercializado de métodos de ouro coloidal usado como reagente de referência, em comparação da detecção do reagente de Baysen com o reagente de referência:
| Baysen Resultado de AV | Resultado do teste do reagente de referência | Taxa de coincidência positiva: 98,54% (95% CI 94,83% ~ 99,60%)) Taxa de coincidência negativa: 100,00% (95% CI 97,31% ~ 100,00%) Taxa total de coincidência: 99,28% (95% CI 97,40% ~ 99,80%) | ||
| Positivo | Negativo | Total | ||
| Positivo | 135 | 0 | 135 | |
| Negativo | 2 | 139 | 141 | |
| Total | 137 | 139 | 276 | |
6. CERTIFICADO
* Certificado do Sistema ISO
* Certificado CE
* Registro da UE
* Registro UCKA MHRA