Kit Diagnostik untuk 25-hidroksi Vitamin D
1. PENGGUNAAN TUJUAN
Kit ini ditujukan untuk deteksi kuantitatif in vitro 25-hidroksi Vitamin D (25-OH Vitamin D) dalam sampel serum/plasma manusia untuk mengevaluasi tingkat Vitamin D. Kit ini hanya memberikan hasil tes 25-hidroksi Vitamin D. Hasil yang diperoleh harus dianalisis dalam kombinasi dengan informasi klinis lainnya.Ini hanya boleh digunakan oleh profesional kesehatan.
2. SPESIFIKASI PRODUK
| Model nomor. | 25-(OH)VD |
| Metodologi | Uji Imunokromatografi Fluoresensi |
| Jenis Sampel | serum/plasma |
| Waktu untuk Hasil | 10-15 menit |
| Penyimpanan | 2~30 ℃/36~86℉ |
| Kehidupan Rak | 24 bulan |
| Sertifikat | ISO13485,CE,MHRA |


| KOMPONEN KIT UTAMA: *Perangkat uji *Sebuah solusi * Tabung B *Petunjuk Penggunaan | Sedang mengemas: *25 tes/kit * Pelabelan tas aluminium foil * bungkus menyusut |
3. METODE PENGUJIAN
| 1 | Bacalah petunjuk penggunaan dan uji manual pengoperasian secara menyeluruh sebelum pengujian dan kembalikan reagen ke ruangan temperatur sebelum pengujian.Jangan melakukan pengujian tanpa mengembalikan reagen ke suhu kamar untuk menghindari mempengaruhi keakuratan hasil tes. |
| 2 | Pilih mode uji standar penganalisa kekebalan portabel WIZ-A101 |
| 3 | Buka paket reagen tas aluminium foil, dan keluarkan perangkat uji; |
| 4 | Masukkan perangkat uji secara horizontal ke dalam slot penganalisa kekebalan; |
| 5 | Di halaman beranda antarmuka operasi penganalisa kekebalan, klik "Standar" untuk masuk ke antarmuka uji; |
| 6 | Klik "QC Scan" untuk memindai kode QR di bagian dalam kit;masukkan parameter terkait kit ke dalam instrumen, dan pilih jenis sampel; Catatan: Setiap nomor batch kit harus dipindai satu kali.Jika nomor batch telah dipindai, lewati langkah ini; |
| 7 | Periksa konsistensi “Nama Produk”, “Nomor Batch”, dll. pada antarmuka pengujian dengan informasi pada label kit; |
| 8 | Setelah konsistensi informasi dikonfirmasi, mulailah menambahkan sampel: langkah 1: Tarik perlahan 30µL sampel serum/plasma sekaligus.Berhati-hatilah untuk tidak menggambar gelembung. Langkah 2: Tambahkan sampel yang diambil ke dalam Larutan (tabung centrifuge transparan), tarik dan tiup sebanyak 3-4 kali (catatan: cairan dalam tutup botol harus ditarik ke dalam botol); Langkah 3: Tambahkan semua larutan campuran dalam larutan A (tabung centrifuge transparan) ke dalam tabung B (tabung centrifuge merah), aduk rata (catatan: pastikan bahwa marker pad terendam dalam cairan), dan inkubasi pada suhu 37℃ selama 8 menit; Langkah 4: Pipet 80µL cairan pada langkah 3 ke dalam lubang sampel alat uji.Hindari menggambar gelembung selama pengambilan sampel. |
| 9 | Setelah penambahan sampel selesai, klik “Waktu” dan sisa waktu pengujian akan ditampilkan secara otomatis di antarmuka. |
| 10 | Penganalisis kekebalan akan secara otomatis menyelesaikan pengujian dan analisis saat waktu pengujian tercapai. |
| 11 | Perhitungan dan tampilan hasil Setelah pengujian oleh penganalisa kekebalan selesai, hasil pengujian akan ditampilkan pada antarmuka pengujian atau dapat dilihat melalui “Riwayat” di halaman muka antarmuka operasi. |
4.KINERJA KLINIS
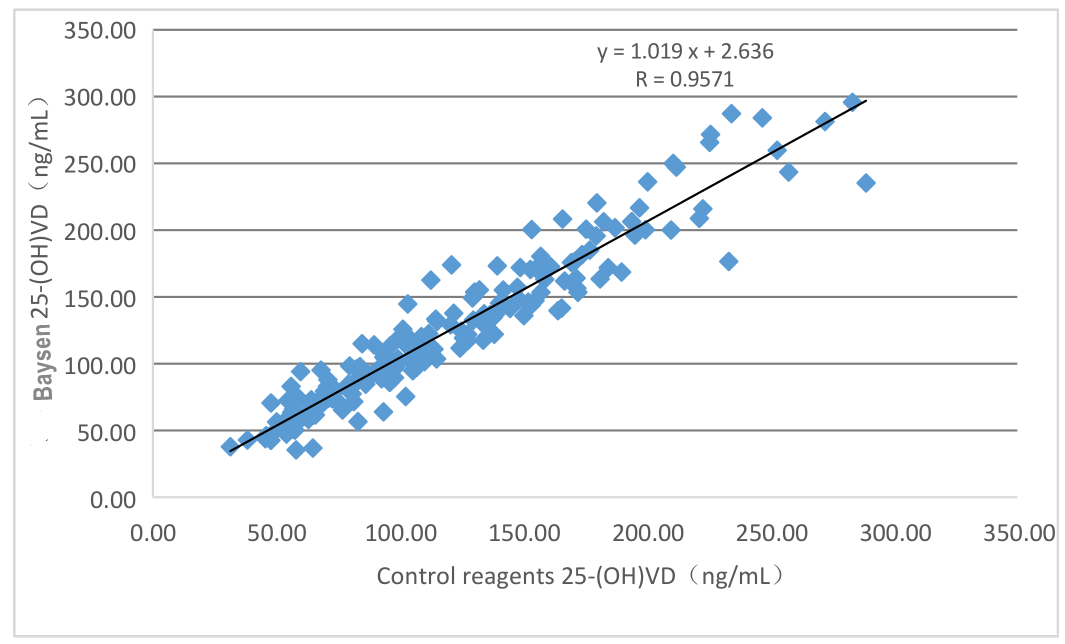
Kinerja evaluasi klinis produk dinilai melalui pengumpulan 196 sampel klinis.Hasilnya dibandingkan dengan menggunakan kit yang sesuai dari kit chemiluminescence yang dipasarkan sebagai reagen referensi.Gunakan regresi linier untuk menyelidiki keterbandingannya.Gunakan regresi linier untuk menyelidiki keterbandingannya.Koefisien korelasi dari kedua tes tersebut masing-masing adalah Y=1,019X-2,636 dan R=0,9571.
5. SERTIFIKAT
* Sertifikat Sistem ISO
* Sertifikat CE
* Pendaftaran UE
* Pendaftaran UCKA MHRA