Kit de prueba rápida de antígeno a adenovirus aprobado por la CE
1. USO PREVISTO
Este kit es aplicable a la detección cualitativa in vitro del antígeno de adenovirus (AV) que pueda existir en una muestra de heces humanas, lo cual es adecuado para el diagnóstico auxiliar de la infección por adenovirus de pacientes con diarrea infantil.Este kit solo proporciona resultados de pruebas de antígenos de adenovirus, y los resultados obtenidos se utilizarán en combinación con otra información clínica para el análisis.Solo debe ser utilizado por profesionales de la salud.
2. ESPECIFICACIONES DEL PRODUCTO
| N º de Modelo. | AV |
| Metodología | Oro Coloidal |
| Tipo de ejemplo | Caras |
| Tiempo hasta el resultado | 10-15 minutos |
| Almacenamiento | 2~30 ℃/36~86 ℉ |
| Duración | 24 meses |
| Certificado | ISO13485, Certificado CE, Certificado UCKA MHRA |

| COMPONENTES PRINCIPALES DEL KIT * Dispositivo de prueba * Tubo de recogida de muestras * Pipeta desechable * Instrucciones de uso | EMBALAJE * 20 pruebas/equipo * Etiquetado de bolsas de papel de aluminio * Envoltura retráctil
|
3. MÉTODO DE PRUEBA
| 1 | Use el tubo de muestreo para la recolección de muestras, la mezcla completa y la dilución para su uso posterior.Use la varilla de prueba para tomar aprox.30 mg de heces, colóquelo en un tubo de muestreo cargado con diluyente de muestra, atornille bien la tapa y agítelo bien para su uso posterior. |
| 2 | En caso de heces finas de pacientes con diarrea, use una pipeta desechable para pipetear la muestra y agregue 3 gotas (aprox. 100 μL) de muestra gota a gota al tubo de muestreo, y agite bien la muestra y el diluyente de la muestra para su uso posterior. |
| 3 | Retire el dispositivo de prueba de la bolsa de papel de aluminio, colóquelo en un banco de trabajo horizontal y marque bien. |
| 4 | Deseche las primeras dos gotas de la muestra diluida, agregue 3 gotas (aprox. 100 μL) de muestra diluida sin burbujas gota a gota al pozo del dispositivo de prueba verticalmente y lentamente, y comience a contar el tiempo. |
| 5 | Interprete el resultado dentro de 10 a 15 minutos, y el resultado de la detección no es válido después de 15 minutos (consulte los resultados detallados en la interpretación de resultados). |
4. EVALUACIÓN Y EXPLICACIÓN DE RESULTADOS
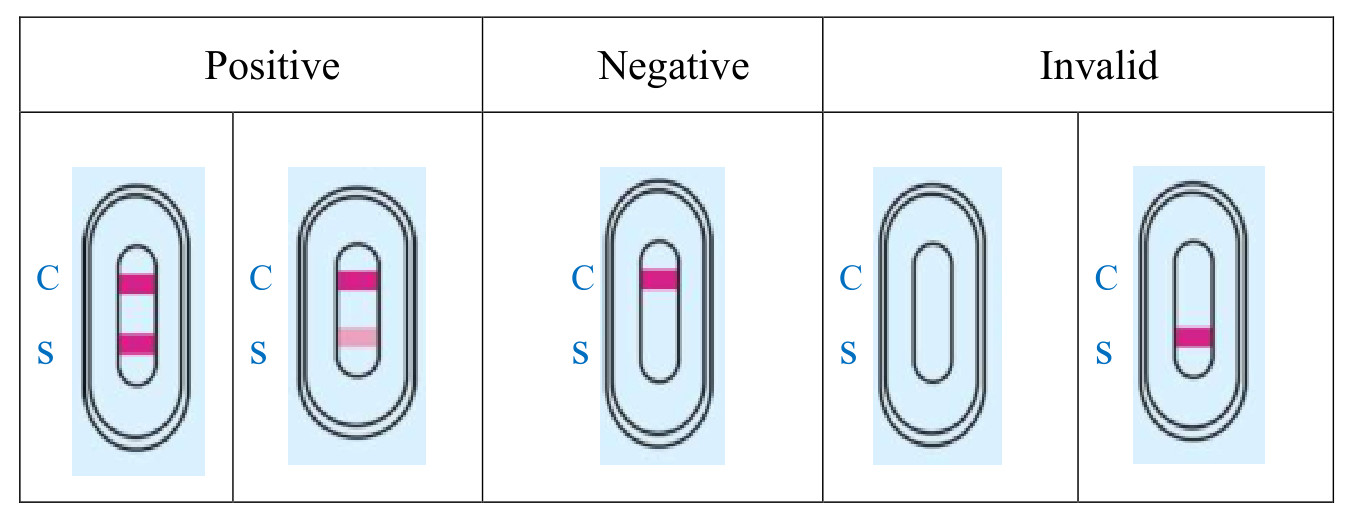
5. RENDIMIENTO CLÍNICO
El rendimiento clínico de este producto se evaluó mediante la recolección de 276 casos de muestras clínicas.Kit comercializado de métodos de oro coloidal utilizado como reactivo de referencia, en comparación con la detección del reactivo de Baysen con el reactivo de referencia:
| Resultado de Baysen de AV | Resultado de la prueba del reactivo de referencia | Tasa de coincidencia positiva: 98,54 % (95 % IC 94,83 %~99,60 %)) Tasa de coincidencia negativa: 100,00 % (95 % IC 97,31 %~100,00 %) Tasa de coincidencia total: 99,28 % (95 % IC 97,40 %~99,80 %) | ||
| Positivo | Negativo | Total | ||
| Positivo | 135 | 0 | 135 | |
| Negativo | 2 | 139 | 141 | |
| Total | 137 | 139 | 276 | |
6. CERTIFICADO
* Certificado del sistema ISO
* Certificado CE
* Registro UE
* Registro UCKA MHRA