Rotavirus- und Adenoviren-Antigen-Kombi-Nachweiskit
1. VERWENDUNGSZWECK
Dieses Kit eignet sich für den qualitativen Nachweis von Spezies-A-Rotavirus- oder Adenovirus-Antigenen, die möglicherweise in menschlichen Stuhlproben vorhanden sind, und eignet sich zur Hilfsdiagnose von Spezies-A-Rotavirus- und Adenovirus-Infektionen bei Patienten mit infantilem Durchfall.Dieses Kit liefert nur Testergebnisse für Rotavirus- und Adenovirus-Antigene der Spezies A. Die erhaltenen Ergebnisse müssen in Kombination mit anderen klinischen Informationen für die Analyse verwendet werden.Es darf nur von medizinischem Fachpersonal verwendet werden.
2. PRODUKTSPEZIFIKATION
| Modell Nr. | Wohnmobil/AV |
| Methodik | Latex |
| Beispielstyp | Gesichter |
| Zeit bis zum Ergebnis | 10-15 Min |
| Lagerung | 2~30 ℃/36~86℉ |
| Haltbarkeit | 24 Monate |
| Zertifikat | ISO13485, CE-Zertifikat, UCKA MHRA-Zertifikat |

| HAUPTKOMPONENTEN DES KITS * Testgerät * Probensammelröhrchen * Einwegpipette * Gebrauchsanweisung | VERPACKUNG * 20 Tests/Kit * Etikettierung von Aluminiumfolienbeuteln * Schrumpffolie
|
3. TESTMETHODE
| 1 | Verwenden Sie das Probenröhrchen zur Probenentnahme, zum gründlichen Mischen und zur Verdünnung für die spätere Verwendung.Benutzen Sie einen Proof-Stick, um ca.Geben Sie ca. 30 mg Stuhl in ein mit Probenverdünnungsmittel gefülltes Probenröhrchen, schrauben Sie den Deckel fest und schütteln Sie es zur späteren Verwendung gründlich. |
| 2 | Bei dünnem Stuhl von Patienten mit Durchfall verwenden Sie zum Pipettieren der Probe eine Einwegpipette, geben Sie 3 Tropfen (ca. 100 μl) der Probe tropfenweise in das Probenröhrchen und schütteln Sie die Probe und das Probenverdünnungsmittel zur späteren Verwendung gründlich. |
| 3 | Nehmen Sie das Testgerät aus dem Aluminiumfolienbeutel, legen Sie es auf eine horizontale Werkbank und markieren Sie es sorgfältig. |
| 4 | Entsorgen Sie die ersten zwei Tropfen der verdünnten Probe, geben Sie 3 Tropfen (ca. 100 μl) der blasenfreien verdünnten Probe tropfenweise vertikal und langsam in die Vertiefung des Testgeräts und beginnen Sie mit der Zeitzählung. |
| 5 | Interpretieren Sie das Ergebnis innerhalb von 10–15 Minuten. Das Erkennungsergebnis ist nach 15 Minuten ungültig (siehe detaillierte Ergebnisse in der Ergebnisinterpretation). |
4. ERGEBNISBEWERTUNG UND ERKLÄRUNG
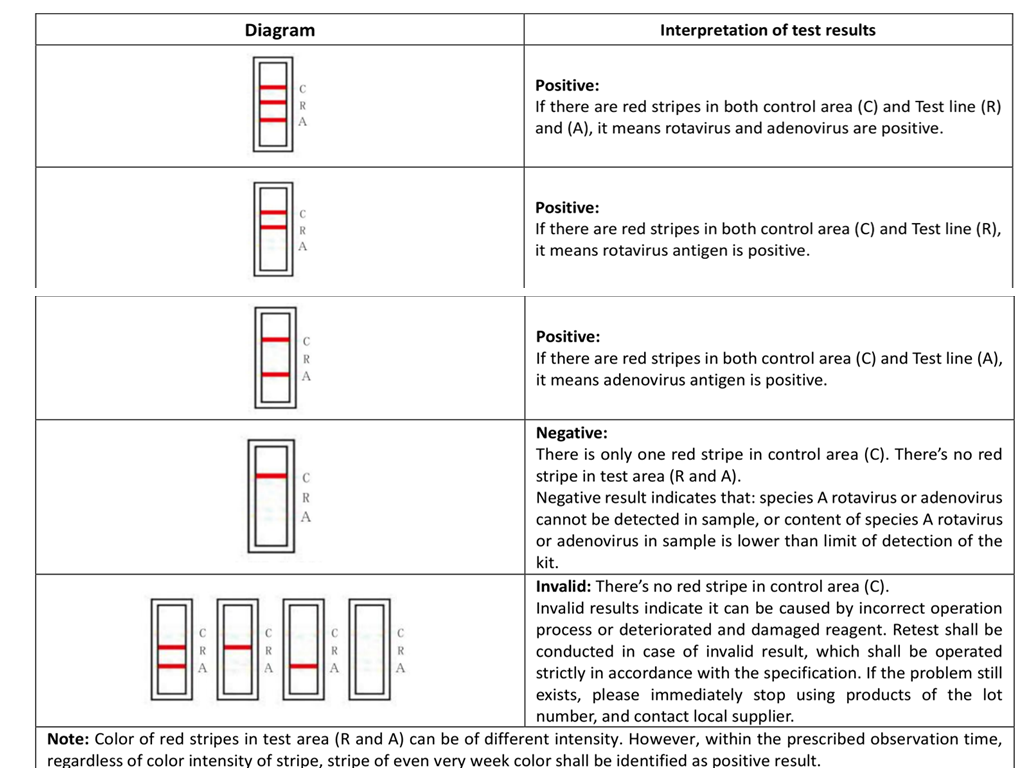
5.KLINISCHE LEISTUNG
Die klinische Leistung dieses Produkts wurde anhand der Sammlung klinischer Proben aus 293 Fällen beurteilt.Zu den Probengebern zählen Patienten, die mit dem Rotavirus und Adenovirus der Spezies A infiziert sind, sowie normale Probanden.Vermarktetes Kit mit kolloidalen Goldmethoden, das als Referenzreagenz verwendet wird.Im Vergleich der BAYSEN-Reagenzerkennung mit Referenzreagenz:
| Baysen-Ergebnis von RV/AV | Testergebnis des Referenzreagenzes | Positive Zufallsrate: 99,36 % (95 % KI 96,48 % ~ 99,89 %) Negative Koinzidenzrate: 100,00 % (95 % KI 97,25 % ~ 100,00 %) Gesamtkoinzidenzrate: 99,66 % (95 % KI 98,09 % ~ 99,94 %) | ||
| Positiv | Negativ | Gesamt | ||
| Positiv | 156 | 0 | 156 | |
| Negativ | 1 | 136 | 137 | |
| Gesamt | 157 | 136 | 293 | |
6. ZERTIFIKAT
* ISO-Systemzertifikat
* CE-Zertifikat
* EU-Registrierung
* UCKA MHRA-Registrierung